酒精是人们生活中的重要饮料,但事实上,饮酒不仅对身体无益,而且会增加肝脏、心血管、神经系统等各部位疾病风险,增高死亡率;长期饮酒还会影响生物钟和人体的正常代谢。
长期饮酒是如何对多种脏器和全身健康产生影响的呢?
美国加州大学洛杉矶分校医疗中心病理学教授French, S. W.为我们深度剖析了长期酗酒的危害及其深层机制[1],文章中提及,在长期大量饮酒情况下,NAD+水平下降,影响了肝脏以及其它脏器的正常功能,扰乱了机体的昼夜节律和代谢水平,引发了酒精性脂肪肝以及其他脏器疾病和全身性疾病。本文是对这篇综述的概括、解读和延伸。
NAD+是哺乳动物体内的保护分子,与DNA修复、能量代谢、组织再生、神经保护和机体寿命等都有密切关联,其含量随着年龄增长而下降[2-4]。

1.过量饮酒使NAD+水平下降
科学家首先介绍了大量饮酒条件下,机体NAD+水平下降的原因。研究人员指出,过量饮酒,血中酒精浓度较高时,NAD+在酒精脱氢酶的作用下转化为还原态NADH,NAD+水平的下降使其无法发挥重要的生物学作用,进而引发一系列病理生理过程[4]。
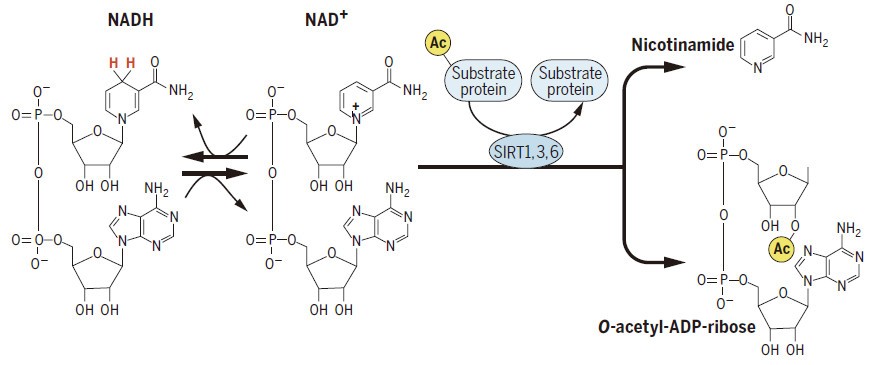
NAD+可以作为共同的辅基质和辅酶,当NAD+转化为NADH时,SIRT1的活性进而下降,将无法发挥重要的生物学作用(图片来自Verdin 2015 Science)
2.NAD+下降可引发酒精性脂肪肝
科学家随后介绍了NAD+下降对肝脏的影响。NAD+通过SIRT1(一种长寿蛋白,在机体的代谢、抗炎等诸多生理过程中发挥重要作用)发挥作用。NAD+含量下降会使SIRT1活性减弱,各种异常蛋白在肝脏中聚积,不但诱发了肝脏的炎症反应,而且使肝脏中脂肪生成增加而消耗减少,造成肝脏脂肪堆积,最终诱发酒精性脂肪肝[5]。
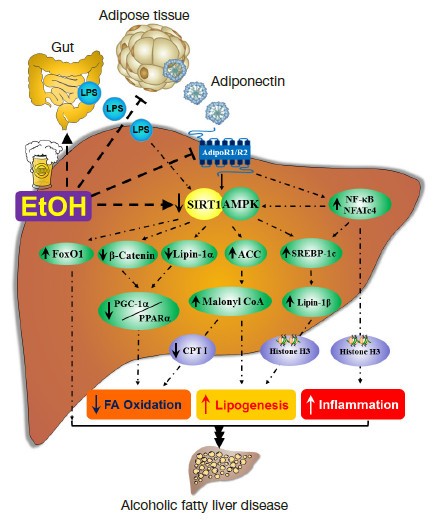
NAD+水平下降,使SIRT1活性下降,通过一系列通路最终引发脂肪肝(图片来自You et.al 2015, Hepatobiliary Surg Nutr)
3.NAD+水平下降扰乱了机体的生物钟和正常代谢
研究人员指出,NAD+含量水平下降会导致SIRT1和SIRT3(参与生物钟的调控)的活性减弱,致使多种重要的生物钟蛋白(例如PER2和CLOCK蛋白)无法正常合成[6],最终引起机体的生物钟紊乱和昼夜节律失调,机体生物钟的紊乱进而影响了正常的代谢过程[7],从而引发代谢异常。

4.NAD+下降对全身健康的影响
科学家最后论述了过量饮酒对全身健康的影响。在大量饮酒时,血液中酒精浓度较高,NAD+将在酒精脱氢酶作用下还原为NADH,而酒精脱氢酶广泛存在于肺部、大脑、胃部、肾脏、食管、直肠、胰腺、小肠结肠、唾液腺、前列腺、甲状腺、肾上腺、脂肪组织、皮肤、乳腺和胆囊中[1]。因此全身性的NAD+下降会加速衰老、引发糖尿病、骨质疏松、心血管疾病、智力减退,并且增高癌症风险。
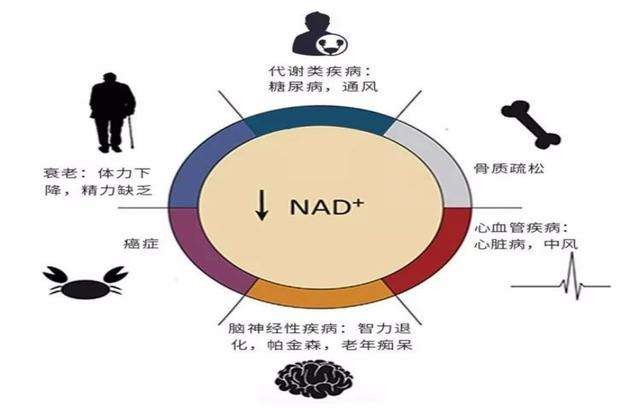
French, S. W.教授的研究详细讲述了长期酗酒降低NAD+水平进而影响肝脏和其他脏器的机制。正如教授所言“酒精脱氢酶存在于身体的所有脏器中,因此在大量饮酒时,这些脏器的NAD+水平会出现全面下降”。NMN(烟酰胺单核苷酸),作为NAD+的前体,可以提高机体NAD+水平,那么NMN能否成为脂肪肝的有效干预手段呢?有研究表明,NMN能够明显改善小鼠的非酒精性脂肪肝水平,提高小鼠代谢水平,维护肥胖小鼠血糖[8]。但是NMN对酒精性脂肪肝的治疗效果,我们仍需要拭目以待。
[1] S.W. French, Chronic alcohol binging injures the liver and other organs by reducing NAD⁺levels required for sirtuin's deacetylase activity, Exp Mol Pathol 100(2) (2016) 303-6.
[2] P. Belenky, K.L. Bogan, C. Brenner, NAD+ metabolism in health and disease, Trends Biochem. Sci. 32(1) (2007) 12-9.
[3] H. Zhang, D. Ryu, Y. Wu, K. Gariani, X. Wang, P. Luan, D. D'Amico, E.R. Ropelle, M.P. Lutolf, R. Aebersold, K. Schoonjans, K.J. Menzies, J. Auwerx, NAD(+) repletion improves mitochondrial and stem cell function and enhances life span in mice, Science 352(6292) (2016) 1436-43.
[4] E. Verdin, NAD⁺in aging, metabolism, and neurodegeneration, Science 350(6265) (2015) 1208-13.
[5] M. You, A. Jogasuria, C. Taylor, J. Wu, Sirtuin 1 signaling and alcoholic fatty liver disease, Hepatobiliary Surg Nutr 4(2) (2015) 88-100.
[6] G. Asher, D. Gatfield, M. Stratmann, H. Reinke, C. Dibner, F. Kreppel, R. Mostoslavsky, F.W. Alt, U. Schibler, SIRT1 regulates circadian clock gene expression through PER2 deacetylation, Cell 134(2) (2008) 317-28.
[7] C.B. Peek, A.H. Affinati, K.M. Ramsey, H.Y. Kuo, W. Yu, L.A. Sena, O. Ilkayeva, B. Marcheva, Y. Kobayashi, C. Omura, D.C. Levine, D.J. Bacsik, D. Gius, C.B. Newgard, E. Goetzman, N.S. Chandel, J.M. Denu, M. Mrksich, J. Bass, Circadian clock NAD+ cycle drives mitochondrial oxidative metabolism in mice, Science 342(6158) (2013) 1243417.
[8] G.M. Uddin, N.A. Youngson, D.A. Sinclair, M.J. Morris, Head to Head Comparison of Short-Term Treatment with the NAD(+) Precursor Nicotinamide Mononucleotide (NMN) and 6 Weeks of Exercise in Obese Female Mice, Front. Pharmacol. 7 (2016) 258.





 京公网安备 11010502041107号
京公网安备 11010502041107号